|
Artículo
|
|
1.- INTRODUCCIÓN - JUSTIFICACIÓN. ANÁLISIS DE LA SITUACIÓN Y/O ESTADO ACTUAL DEL TEMA
El trasplante de médula ósea es el tratamiento de elección de diversas enfermedades hematológicas, oncológicas, congénitas e inmunodeficiencias, reservado para aquellos pacientes que no tienen otra posibilidad de tratamiento.1,2
Según la Organización Nacional de Trasplantes, en 2012 se ha vuelto a conseguir un máximo histórico de Trasplantes de Médula Ósea en España, acusándose un aumento progresivo desde 2006. Concretamente, la cifra de trasplantes realizados en 2012, alcanza los 2.699, de los que 271 han sido pediátricos. Cabe destacar las Comunidades Autónomas (CCAA) que más trasplantes por millón de población han realizado: Cantabria, seguida por Navarra, Asturias y Murcia. El Hospital Universitario Marqués de Valdecilla, en Cantabria, es uno de los nueve centros de referencia para el trasplante de médula ósea pediátrico en España, y en él se realizaron 68 trasplantes en el año 2012, de los cuales 3 fueron pediátricos.3
Este proceso no está exento de riesgos y situaciones potencialmente estresantes que deben afrontar los pacientes y sus familiares.2,4,5 El paciente y su familia deben conocer que este procedimiento desencadena un estado de compromiso múltiple de órganos, tejidos y depresión inmunológica severa, predisponiendo a infecciones y a efectos secundarios como consecuencia de tratamientos potencialmente tóxicos. Por todo ello, estos pacientes susceptibles de trasplante requieren tanto del apoyo profesional, como familiar, para sentirse seguros durante las etapas del tratamiento.6
Si añadimos que el afectado por la enfermedad es un niño, se altera el funcionamiento familiar.7 Todos son sensibles al sufrimiento de un niño, ya que las necesidades de los niños son únicas y requieren especial atención cuando se presenta una enfermedad.8 Ocurren largas y frecuentes hospitalizaciones, largos tratamientos, separación de la familia, cambios físicos e inmunitarios y riesgo de retraso en el desarrollo psicomotor y escolar. El niño y sus familiares tendrán que enfrentarse a muchos desafíos emocionales e interpersonales a lo largo del tratamiento. Por lo que en cada etapa, habrá que cuidar su mente tanto como su cuerpo. Esto hace necesario una buena coordinación del equipo multidisciplinar.7,8
2.- OBJETIVOS
El objetivo principal es:
- Actualizar los conocimientos sobre el Trasplante de Médula Ósea (TMO).
Y los objetivos específicos:
- Describir los conceptos más importantes sobre el TMO
- Desarrollar las fases del TMO y su seguimiento
- Capacitar al personal enfermero para proporcionar ayuda oportuna que mejore la adaptación del niño y su familia al proceso de TMO.
3.- METODOLOGÍA
El presente trabajo es una monografía con el propósito de registrar y sintetizar el conocimiento actual sobre el tema propuesto. Han sido empleadas diversas bases de datos como: PUBMED, CUIDEN, ENFISPO, SCIENCE DIRECT, GOOGLE SCHOLAR y FISTERRA, de las que se localizaron diversos artículos.
También se realizó búsqueda de información en diversas asociaciones y entidades públicas: GELTAMO; REDMO; Ministerio de Sanidad y Consumo; Hospital Universitario Marqués de Valdecilla (HUMV); Sociedad Española de Hematología y Oncología Pediátrica (SEHOP) y de la Organización Nacional de Trasplante (ONT).
Para esta monografía se realizó búsqueda bibliográfica entre octubre del 2011 y febrero del 2012, no obstante, se revisó posteriormente la memoria de TPH en España y Cantabria de la que se habla en la introducción, no siendo posible referenciar los datos correspondientes al año 2013 ya que la ONT aún no ha publicado la memoria relativa al pasado año.
Una vez concluida la muestra y posterior lectura de los artículos, algunos de los criterios de exclusión que se siguieron fueron la antigüedad de la publicación y artículos de foros de opinión en lugar de revistas científicas.
4.- ANÁLISIS DE LOS RESULTADOS
Conceptos básicos sobre el trasplante de progenitores hematopoyéticos
La indicación más frecuente en el paciente pediátrico es la Leucemia Aguda (62%), seguido por condiciones no malignas: enfermedades congénitas e inmunodeficiencias (36%). 1,9,10
- Clasificación de los trasplantes de progenitores hematopoyéticos
Existen tres clasificaciones diferentes:
A) Según el tipo de Donante
- Autólogo: Las células madreproceden del propio paciente. Se obtienen cuando el paciente ha respondido al tratamiento de su enfermedad, se dice que se encuentra en remisión completa. Es más sencillo que el trasplante alogénico y con menos complicaciones.8,10
- Alogénico: Las células madre proceden de otro individuo. Habitualmente el donante es un familiar del paciente, no obstante, cuando no existe parentesco entre donante y receptor se dice que es un trasplante de donante no emparentado.4,8,10
B) Según el origen de las células madre
- Médula ósea: es la forma clásica de obtención. Se obtiene del interior de las crestas iliacas.
- Sangre periférica: Mediante aféresis (proceso que separa las células madre).
- Sangre de cordón umbilical: rica en células madre.
De ahí que se prefiera utilizar el término de “trasplante de progenitores hematopoyéticos” (TPH) porque incluye todos los tipos de trasplante: médula ósea, sangre periférica y cordón umbilical.10
C) Según el tipo de acondicionamiento
Es el tratamiento que recibe el paciente como preparación para el trasplante.
Distinguimos dos clases:9,10
- Mieloablativo: Dosis altas de quimioterapia, asociada o no a radioterapia. El empleo o no de la radioterapia lo discuten los hematólogos responsables del paciente en sesión teniendo en cuenta determinados factores: las características de la enfermedad, si es una recaída precoz, si el paciente ha recibido ya radioterapia, si aún hay enfermedad residual o el estado general del paciente antes del trasplante.
- De intensidad reducida: Administración de potentes inmunodepresores asociados a quimioterapia, no a dosis tan altas como en el mieloablativo.
- Compatibilidad del donante
Esta compatibilidad se estudia mediante el análisis de una muestra de sangre del paciente y del posible donante.
Todo individuo hereda la mitad de estos antígenos de su padre y la otra mitad de su madre, por ello la probabilidad de que los progenitores sean compatibles es mucho menor que la referida a un hermano. Existe una probabilidad del 25% de que un hermano del paciente sea perfectamente compatible con su tipo de Antígeno Leucocitario Humano (HLA). 8
El grupo de donantes alternativos a los familiares está constituido por donantes voluntarios recogidos en diversos registros internacionales, donde actualmente hay registrados más de 14 millones de donantes y unidades de cordón en todo el mundo. En España, el registro existente es el REDMO: Registro de Donantes de Médula ósea, creado en 1991 por la Fundación Internacional Josep Carreras.10
El apoyo a los donantes es importante antes y después de la donación particularmente con los donantes emparentados, que conocen al receptor y probablemente continúen involucrados, o al menos informados, con su evolución.4,8
- Fases del trasplante hematopoyético
RECEPTOR
Se realizarán una serie de estudios analíticos, radiológicos y funcionales necesarios para determinar el estado de salud del paciente, el grado de control de la enfermedad y, en función de los resultados, decidir si el paciente es APTO para el trasplante, y en caso afirmativo cuál es el procedimiento terapéutico más adecuado.11
DONANTE
Existirá cuando hablemos de trasplante alogénico. Se someterá también a una serie de estudios analíticos, preoperatorios y, si la donación es de sangre periférica, a una valoración por el equipo de la unidad de aféresis.10,12
- Firma del consentimiento informado
En pacientes menores de 18 años, debe ser firmado por sus tutores legales tras haber informado adecuadamente al menor y oída su opinión, según legislación vigente(Ley 41/2002, de 14 de noviembre, básica reguladora de la autonomía del paciente y de derechos y obligaciones en materia de información y documentación clínica).13
- Ingreso en la unidad de trasplante
Unidad de TPH: recibe esta denominación el área del hospital dotada de personal médico y de enfermería específicamente preparada para la obtención, manipulación y administración de progenitores hematopoyéticos, así como para prevenir y tratar complicaciones del TPH.9
El ingreso se inicia siete días antes de la fecha fijada para el trasplante, estees el momento en que se da la separación de la familia y el hogar. El papel de enfermería, en esta etapa, se centra en facilitar la adaptación al medio hospitalario, disminuir el estrés y mejorar la respuesta al tratamiento mediante la recepción e información detallada al paciente y familia sobre las normas internas del servicio, horarios de visita, participación familiar, objetos personales y actividad física y ocupacional durante el ingreso.9,14
Durante el ingreso y antes de comenzar el acondicionamiento, es necesario canalizar un catéter venoso central al paciente. Este catéter debe permitir la administración de citostáticos, progenitores hematopoyéticos, líquidos electrolitos, antimicrobianos, inmunosupresores, soporte hemoterápico y nutrición parenteral, así como la obtención de muestras de sangre. El acceso venoso más frecuente es la vena subclavia y es del tipo Hickman, los reservorios subcutáneos no son útiles para el TPH ya que no están diseñados para perfusiones continúas, son de una sola luz y de flujo limitado. Este acceso venoso se mantendrá durante el tiempo que se considere oportuno, incluso siendo dados de alta a su domicilio portando el catéter. 9,15
Su finalidad es:
- Eliminar células anómalas del organismo.
- Hacer espacio en la médula ósea para nuevas células.
- Evitar el rechazo de las nuevas células por parte del receptor.
La duración es variable: entre dos y siete días. A partir de esta fase comienza la parte más complicada física y psicológicamente del proceso para el niño y será imprescindible atender las necesidades emocionales y afectivas de éste y de su familia.10,14
A los 5-7 días de iniciado el acondicionamiento deberemos tener en cuenta que es muy probable que aparezca mucositis en el niño: es la inflamación de la mucosa de la boca y desaparece cuando se recuperan cifras hematológicas. Es la complicación más molesta para el paciente, ya que es doloroso y evita la adecuada ingestión de alimentos.
Cuando la ingestión de alimentos se ve muy limitada, y esto ocurre en gran mayoría de ocasiones, la alimentación deberá administrarse por vía endovenosa (nutrición parenteral).10 La incidencia de esta complicación va a depender mucho del acondicionamiento que reciba el niño, así como del tipo de trasplante. Por eso siempre será mayor en un trasplante alogénico que en un autotrasplante. Cuando se utilicen fármacos de alta intensidad así como irradiación corporal total, podemos hablar de una incidencia entre el 75 y el 100% de los casos.9
- Día 0: infusión de progenitores hematopoyéticos
A nivel internacional se ha decidido señalar el día de la infusión como día 0 y los días posteriores en positivos, para así reconocer en qué momento del trasplante nos encontramos sólo con mirar el día. La infusión se realiza de forma similar a una trasfusión sanguínea. Dura entre 30 minutos y dos horas durante las cuales, la enfermeravigila las constantes vitales del paciente y la aparición de efectos secundarios. 10,14,16 (Figura 1)
Figura 1
- Post-trasplante inmediato
Son los 15-20 días después del trasplante, en los que el paciente permanece aislado con dieta de baja carga bacteriana, cocinada a altas temperaturas. Son dietas especiales que tienen incorporados los hospitales donde existe una unidad de trasplantes de médula.
Las posibles complicaciones inmediatas son la infección y la hemorragia, por lo cual el cuidado del paciente debe centrarse en su prevención y tratamiento precoz. Tanto en esta fase como en todas las demás, la enfermera deberá valorar el dolor del paciente, siendo la escala más frecuentemente utilizada la Escala Visual Analógica para pacientes pediátricos. 10,16,17 (Figura 2)
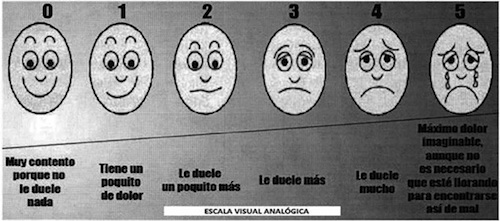
Figura 2
Esta fase finaliza cuando las células germinales trasfundidas migran hacia la médula ósea del receptor y comienzan a regenerarse.10,16
Los pacientes sometidos a TPH son dados de alta cuando superan el período de aislamiento, toleran la vía oral y su situación clínica y los tratamientos que debe recibir permiten un seguimiento ambulatorio. Tras un TPH alogénico, los pacientes tienen un control estrecho, como mínimo semanal, durante la fase inicial. En estas visitas se reajustará su tratamiento farmacológico, que consistirá básicamente en inmunosupresores, corticoides, antibacterianos y/o antivíricos, así como fármacos específicos para cualquier complicación que pueda surgir durante y después del proceso.
Es importante que el paciente sepa que necesitará un tiempo para volver a su estado físico previo a la enfermedad y al trasplante. Reintegrarse a la vida fuera del hospital es un gran paso. La readaptación puede ser un proceso largo.8,10,18
La enfermera debe explicar una serie de recomendaciones a los familiares del niño cuando se prevea el alta hospitalaria:10
- Evitar alimentos crudos y sin cocinar, leche no pasteurizada, quesos frescos, yogur, agua no embotellada y frutas y verduras sin lavar.
- Deben beber un mínimo de 2 litros de agua al día.
- No tomar alcohol ni fumar (adolescentes).
- Evitar aglomeraciones (metro, autobús, salas de espera, etc.) y en caso de ser imposible, utilizar mascarilla.
- Evitar el contacto con otros niños con enfermedades exantemáticas (sarampión, varicela, etc.) y con niños recién vacunados.
- Deberán evitar el contacto con personas que presenten cuadros catarrales.
- Evitar el contacto con animales de compañía, especialmente, si no están vacunados.
- Hacer ejercicio cada día (juegos habituales, bicicleta, etc.), evitando exponerse al sol.
- Pesar al niño al menos una vez por semana en la misma báscula.
- Vigilar la temperatura axilar dos veces al día.
- Deben tomar toda la medicación prescrita.
- Máxima higiene personal.
Además, los padres deben conocer los signos de alarma que hacen que deban acudir a urgencias:19
- Diarrea que no desaparece o se presenta con sangre.
- Náuseas intensas, vómitos o inapetencia.
- Incapacidad para comer o beber.
- Debilidad extrema.
- Enrojecimiento, hinchazón o exudado de los accesos venosos de los que el niño sea portador.
- Dolor en el área del estómago.
- Fiebre, escalofríos o sudores.
- Aparición de una nueva erupción cutánea, ampolla, lesión o enrojecimiento de la piel.
- Ictericia, prestar atención a la piel y la esclerótica.
- Dolor de cabeza fuerte o que no desaparece.
- Tos que empeora progresivamente.
- Problemas para respirar cuando está en reposo o realizando tareas simples.
- Disuria.
En cada visita se realiza un análisis de sangre que permite comprobar que la médula está funcionando correctamente y permite detectar precozmente posibles complicaciones. En estas visitas, además, se vigila muy estrechamente la posibilidad de que estos pacientes sufran Enfermedad de Injerto Contra Huésped (EICH) agudo (es una de las complicaciones más frecuentes), producida por los linfocitos del donante. Esta enfermedad puede afectar diferentes órganos como la piel, el hígado y el intestino, en cada uno de los cuales tendrá diferentes manifestaciones: desde eritemas en la piel, aumentos de bilirrubina en sangre por afectación hepática, hasta diarrea y dolor abdominal por afectación intestinal. Por este motivo se dan las recomendaciones a los padres y se les informa de los signos de alarma que deben vigilar (control de la piel, diarreas, fiebre, ictericia, etc.)9
Se previene mediante el empleo de fármacos inmunosupresores, cuya duración es muy variable, desde 3 a 6 meses hasta 1 o 2 años.
No obstante, estudios recientes demuestran que los casos leves de EICH parecen tener un efecto beneficioso en el tratamiento de Leucemias y Linfomas. En estas enfermedades, el índice de recaída es más bajo en pacientes con TPH que presentaron un EICH leve. Los hematólogos estudian, en cada trasplante, la forma de maximizar este efecto, sin aumentar el riesgo para el paciente.8,10
El seguimiento mínimo recomendado es de cinco años tras el trasplante.
A largo plazo, se deben tener en cuenta otros factores como: EICH crónico (se considera a partir del tercer mes tras el trasplante), el elevado riesgo de padecer infertilidad, segundas neoplasias, cataratas (especialmente si se ha recibido irradiación corporal total) y las vacunaciones, ya que el paciente ahora tiene un nuevo sistema inmunitario, por lo que habrá que revacunar al paciente de nuevo.
El trasplante pediátrico, por su elevado riesgo endocrinológico precisa un estrecho seguimiento para vigilar su afectación en el crecimiento.10,20
ASPECTOS EMOCIONALES Y SOCIALES EN EL NIÑO Y SU FAMILIA DURANTE EL PROCESO
Desde el momento del diagnóstico y de una afección grave, como lo es el TMO y a lo largo del proceso de la enfermedad, el paciente presentará reacciones psicológicas asociadas a ese diagnóstico: se generan miedos relacionados con la posibilidad de no encontrar un donante compatible, a las pruebas médicas y/o complicaciones del tratamiento, a la progresión de la enfermedad y a las secuelas a largo plazo. Todos estos factores relacionados con el proceso del trasplante producirán un impacto en su salud emocional, verán interrumpidas sus tareas cotidianas (tanto del niño, como de la familia) y crearán expectativas poco realistas sobre el tiempo de regreso a la “normalidad”. Dichas reacciones son normales y necesarias para llegar al afrontamiento y la adaptación psicológica. Sin embargo, se estima, que un 25% de pacientes y/o familiares que se sometan al TMO presentarán alteraciones psicopatológicas que requerirán una atención especializada. Las más frecuentes serán sintomatología depresiva o ansiosa de intensidad leve/moderada.9
El TMO es, por tanto, un proceso asociado a elevada morbilidad psicológica/psiquiátrica, por lo que es recomendable evaluar los riesgos psicosociales individuales para minimizar el riesgo de desadaptación psicológica del paciente y su familia, optimizar la calidad de vida y favorecer una mejor adherencia terapéutica1, ya que estos factores psicosociales tienen un papel significativo en la recuperación y readaptación a la vida a largo plazo tras haber recibido un TMO.8
FACTORES DE VULNERABILIDAD PSICOLÓGICA
Psicosociales9
- Edad joven (Adolescencia).
- Antecedentes psiquiátricos.
- Ansiedad ante el tratamiento y los procesos médicos.
- Enolismo o consumo de tóxicos (recordemos que hablamos de edades comprendidas entre los 0 y 18 años).
- Bajo apoyo socio-familiar percibido.
- Mal afrontamiento previo de la enfermedad.
- Presencia de importantes estresores vitales concurrentes.
Asociados a la enfermedad y tratamiento9
- Enfermedad de larga evolución.
- Enfermedad avanzada y/o terminal.
- Afectación funcional importante.
- Dolor.
- Fatiga.
Se realizan una serie de estudios médicos antes de realizar un TMO como hemos visto en el capítulo anterior, pero también es importante hacer un análisis de factores psicosociales en la medida de reducir problemas relacionados con la no adaptación a la nueva situación.
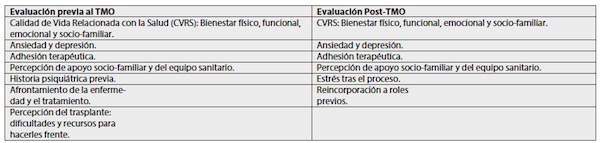
Existe una escala definida para niños (entre 1 y 16 años), que nos permite en cierta manera objetivar el estado de ánimo del niño: la Escala de LANSKY, en la cual hay un orden decreciente entre 100 y 0, donde 100 es el valor máximo que se le puede dar a la actividad y el juego del niño.21
En los niños, hemos de saber además que al enfrentarse a este proceso, existirá una mayor dependencia de sus padres, una dificultad en la reanudación de las actividades apropiadas para su edad o incluso alteraciones permanentes en su desarrollo.1
Aunque el funcionamiento cognitivo y comportamiento estén dentro de la “normalidad”, los niños entran en el hospital con un elevado nivel de estrés, el cuál aumentará drásticamente durante el acondicionamiento.1 Los días de mayor vulnerabilidad coincidirán con el período de aplasia producido por los citostáticos, cuando la sintomatología física se muestra en su mayor intensidad: mucositis, fiebre, astenia, anorexia, náuseas, vómitos y hemorragias.Por todo ello, el aislamiento protector puede tener importantes efectos psicológicos en el paciente.4,5
En general, las instituciones hospitalarias con unidades de TMO permiten la compañía de un familiar durante todo el proceso de aislamiento, desde el momento del ingreso hasta el alta.6 Además, lograr que su habitación en el hospital sea lo más cómoda posible puede ayudarlo a enfrentar mejor la situación. En muchos centros le permitirán traer cosas personales como juguetes o ropa, algunos pueden tener restricciones o requerir que los elementos sean previamente esterilizados. Algunos objetos que podrían servir de ayuda a los niños y se les podría aconsejar a su padres traer son sus juguetes favoritos, videojuegos, elementos de dibujo y manualidades, su manta favorita, un diario, libros escolares y los planes de clase, una radio, libros o revistas, una libreta con direcciones y teléfonos de sus amigos, un ordenador portátil, rompecabezas y pasatiempos.8
A medida que se acerca el alta hospitalaria se comienza a anticipar y preparar al paciente y su familia, para la recuperación paulatina de su vida anterior y para que pueda asumir sus roles progresivamente, anticipando respuestas.5 Pero a veces, se puede vivir como un acontecimiento estresante para el paciente, el cual puede haberse convertido en demasiado dependiente del personal sanitario.12 La enfermera posee un rol fundamental para apoyar al paciente y a la familia en la adaptación de esta nueva etapa y a enfrentar los factores estresantes.6 El mundo externo no ha cambiado apenas, mientras que en el del niño y sus padres se ha generado toda una revolución interna de su universo de valores.5
Los padres de niños con una enfermedad grave, suelen ser descritos como sobreprotectores o restrictivos, y las familias suelen tener conflictos y dificultades para tomar decisiones. Esta sobreprotección puede ser un factor de riesgo para la autoestima de niños enfermos crónicos. Además, la presencia de síntomas depresivos y angustia en los padres son relativamente frecuentes, interviniendo en su salud mental tanto la percepción que tenga la gravedad del estado de su hijo, como también su propia relación de pareja.22 De hecho, un hilo común en muchos estudios de CVRS, es que los padres informan de una calidad significativamente menor, tanto antes como después del TMO en comparación con lo que informan sus hijos. Esto podría explicarse porque el niño informa sobre su condición subjetiva: ellos conocen realmente cómo se sienten, mientras que los padres conjeturan a partir de observaciones y la comunicación con sus hijos. Igualmente, los niños se centran más en el aquí y el ahora, y sus padres en su bienestar futuro.1,23,24
Entre los objetivos del equipo multidisciplinar se deberían de incluir: ayudar a los padres y/o familiares a conservar sus relaciones sociales para no aislarse de las personas, mejorar la comprensión de la enfermedad y las reacciones del niño y reflexionar sobre el difícil proceso emocional del trasplante para adquirir la conciencia de que los sentimientos ambivalentes son normales y esperados. Ayudando a los padres de manera indirecta se presta asistencia al niño.22
En el estudio de Barrera23 (2009), se tomó como muestra una población 99.65% femenina con una media de edad de 8.27 años, antes de recibir el trasplante de células progenitoras y entre 1 y 2 años posteriores, de cuyos resultados se puede extraer que: inmediatamente después del trasplante, todos informan de peor CVRS, sin embargo, existe una mejora física y psicosocial al año del trasplante.
De la lectura bibliográfica realizada para la elaboración de este trabajo, según autores como Tremolada1; Brown4; Carreras9 Tanzi23 y Clarke24, se extraen las siguientes conclusiones:
- Los niños más pequeños muestran menos angustia que los mayores.
- Tras un trasplante autólogo, cabe esperar mejor afrontamiento y readaptación a la vida anterior, ya que se asocia con menos riesgos.
- Se encuentran peores sistemas de adaptación y afrontamiento de la enfermedad cuando pasa mucho tiempo entre el diagnóstico y el momento del TMO. Puede ocurrir cuando el paciente ha sido objeto de un protocolo de tratamiento más largo, lo que conlleva mayores efectos secundarios y secuelas.
- No se observan cambios significativos en el coeficiente intelectual, no obstante, no quiere decir que no se observen cambios respecto a los logros académicos.
- Se encuentran diferencias significativas en la CVRS en los hijos de madres más jóvenes y con menor nivel educativo.
- En los supervivientes a los 5 años del trasplante, se puede decir que la mayoría tienen un buen estado general y están reintegrados a la vida laboral y social, estos son aproximadamente el 89%. Sin embargo, el riesgo de contraer enfermedades y de mortalidad continúa siendo superior.
Será importante identificar las familias vulnerables y proporcionar ayuda oportuna: facilitar la adaptación a la enfermedad, al trasplante y al retorno a su vida normal, sin dejar de lado, en ningún momento, los cuidados de salud que serán necesarios para toda la vida.1,22
5.- DISCUSIONES
Durante la revisión bibliográfica se observó que no existen muchos artículos sobre aspectos emocionales y/o calidad de vida de los niños sometidos a un trasplante de médula ósea. La mayoría de ellos son referidos a oncología pediátrica general, pero no hacia el proceso del trasplante en concreto. La explicación quizá pueda ser que es un procedimiento relativamente novedoso, ya que el primer trasplante alogénico se realizó en 1957, y concretamente en España no se realizaría hasta el año 1976.
No obstante, hay algo en lo que sí coinciden todos los artículos revisados y es que durante un TPH infantil hay que tener muy presentes a las familias de los niños porque analizando cómo actúa su entorno podemos ayudarles a afrontar la enfermedad y sus complicaciones.
6.- CONCLUSIÓN
Todas las medidas encaminadas a la mejoría psicológica de estos pacientes contribuyen a acelerar su recuperación y a mejorar los resultados del trasplante, por lo que conocer las necesidades de la familia y el niño puede ayudarlos a enfrentar esta situación de forma eficaz y positiva, minimizando las consecuencias emocionales.
Es indudable que a lo largo de todo el proceso del trasplante hematopoyético, la colaboración multidisciplinar es fundamental. Por ello, se requiere de un personal con un perfil determinado desde el punto de vista de calidad humana, académica y profesional, que responda a las necesidades de este grupo de pacientes.
Dicha colaboración, implica la participación activa y continua de los cuidados enfermeros sobre la base de conocimientos y experiencias para la innovación e investigación, y por tanto, la búsqueda de mejores alternativas de cuidado y tratamiento para estos pacientes.
Elizabeth M. Tanzi23: “Para reflejar el valor total de cualquier terapia, es necesario evaluar no sólo variables como: supervivencia global, supervivencia libre de enfermedad, morbilidad, mortalidad y coste, sino también la calidad de vida.”
7.- AGRADECIMIENTOS
A la Dra. Mónica López Duarte. Hematóloga del Hospital Universitario Marqués de Valdecilla.
8.- BIBLIOGRAFÍA
- Tremolada M, Bonichini S, Pillon M, Messina C, Carli M. Quality of life and psychosocial sequelae in children undergoing hematopoietic stem-cell transplantation: A review. Pediatr Transplant. 2009;13(8):955-970.
- Barriga F, Baeza R, Pereira J, Besa P, Caldumbide I, Medel M. Trasplante de médula ósea en pacientes pediátricos. Rev Chil Pediatr. 1999;70(3):194-2000
- Organización Nacional de Trasplantes [sede Web]. Madrid: Organización Nacional de Trasplantes; 2010 [acceso 16 de noviembre de 2011]. Memoria TPH 2010. Disponible en: http://www.ont.es/infesp/Memorias/Memoria_tph_2010p1.pdf.
- Brown M. Nursing care of patients undergoing allogeneic stem cell transplantation. Nurs Stand. 2010;25(11):47-56.
- Arranz P, Coca C, Bayés R, Del Rincón C, Hernández-Navarro F. Intervención psicológica en pacientes que deben someterse a un transplante de médula ósea. Psicooncología. 2003;0(1):93-105.
- Matsubara TC, Carvalho EC, Marin SR, Sawada NO. Crisis de la familia en el contexto de trasplante de médula ósea: una revisión integrada. Rev Lat Am Enfermagem. 2007;15(4):665-670.
- Palma C, Sepúlveda F. Atención de enfermería en el niño con cáncer. Rev Ped Elec [revista en Internet] 2005. [acceso 30 de noviembre de 2011];2(2):[37-43]. Disponible en: http://www.revistapediatria.cl/vol2num2/10.htm.
- Bone Marrow [sede Web]. New York: The Bone Marrow Foundation; 2008 [acceso 10 de diciembre de 2011]. Trasplante Alogénico de Médula Ósea o Células Precursoras: Un folleto médico y educativo. Disponible en: http://www.bonemarrow.org/downloads/Sp-AlogenicoFolleto.pdf.
- Carreras E, Rovira M, Martínez C. Manual de Trasplante hemopoyético. 4 ª ed. Barcelona: Antares; 2010.
- Fundación Josep Carreras contra la Leucemia [sede Web]. Barcelona: Fundación Internacional Josep Carreras; 2009 [acceso 1 de diciembre de 2011]. Martínez C, Carreras E. Trasplante de Médula Ósea, Sangre periférica y Sangre de Cordón Umbilical. Guía para el paciente. Disponible en: http://www.fcarreras.org/files/12548.
- López-Duarte M, Insunza A. Valoración pretrasplante del paciente [monografía en Intranet]. Santander: Unidad de Hematología y Hemoterapia del HUMV; 2009 [acceso 30 de noviembre de 2011]. Disponible en: http://portal.intranet.humv.es/index.php?option=com_docman&task=doc_download&gid=2368&mode=view.
- López Duarte M, Insunza A. Valoración del donante [monografía en Intranet]. Santander: Unidad de Hematología y Hemoterapia del HUMV; 2009 [acceso 30 de noviembre de 2011]. Disponible en: http://portal.intranet.humv.es/index.php?option=com_docman&task=doc_download&gid=2370&mode=view.
- Ley Básica Reguladora de la Autonomía del Paciente y de Derechos y Obligaciones en Materia de Información y Documentación Clínica. Ley 41/2002 de 14 de noviembre. Boletín Oficial del Estado, nº 274, (15-11-2002).
- Durán R, Robledo C. Atención protocolizada de enfermería en pacientes pediátricos con trasplante de médula ósea. Rev Enferm Inst Mex Seguro Soc. 2004;12(2):83-88.
- Carrera M, Ruiz J, Escobar L, Agüeros P, Vesga AM, Gómez L, et al. Cuidados, mantenimiento y retirada del catéter de Hickman. Manual de Cuidados y Mantenimiento de catéteres. Santander: Área de Formación y Calidad de Enfermería HUMV; 2000.
- Díez ME, De Juan N. Cuidados de enfermería en el paciente sometido a trasplante de médula. Enferm Glob [Internet]. 2006 [acceso 1 de diciembre de 2011];5(9): [1-19].Disponible en: http://revistas.um.es/eglobal/article/view/373.
- Bárcena MJ, Insunza A. Manejo del dolor por enfermería en el TCPH [monografía en Intranet]. Santander: Unidad de Hematología y Hemoterapia del HUMV; 2009 [acceso 30 de noviembre de 2011]. Disponible en: http://portal.intranet.humv.es/index.php?option=com_docman&task=doc_download&gid=2381&mode=view.
- Bárcena MJ, Insunza A. Actuación de enfermería al ingreso y alta en el TCPH [monografía en Intranet]. Santander: Unidad de Hematología y Hemoterapia del HUMV; 2009 [acceso 30 de noviembre de 2011]. Disponible en: http://portal.intranet.humv.es/index.php?option=com_docman&task=doc_download&gid=2389&mode=view.
- Dugdale D, Zieve D, Chen YB. Alta después de trasplante de médula ósea [monografía en Internet]. Maryland: Medline; 2010 [acceso 10 de diciembre de 2011]. Disponible en: http://www.nlm.nih.gov/medlineplus/spanish/ency/patientinstructions/000010.htm.
- López Duarte M, Insunza A. Seguimiento Post-TCPH del paciente pediátrico [monografía en Intranet]. Santander: Unidad de Hematología y Hemoterapia del HUMV; 2009 [acceso 30 de noviembre de 2011]. Disponible en: http://portal.intranet.humv.es/index.php?option=com_docman&task=doc_download&gid=2375&mode=view.
- Guía de la unidad de trasplante y manual de procedimientos operativos. Salamanca: Unidad de Hematología, Hospital Universitario de Salamanca; 2008.
- Castro EK, Moreno B. Funcionamiento familiar en situación de trasplante de órganos pediátrico. Interam J Psychol. 2005;39(3):383-388.
- Tanzi EM. Health-related quality of life of hematopoietic stem cell transplant childhood survivors: state of the science. J Pediatr Oncol Nurs. 2011;28(4):191-202.
- Clarke SA, Eiser C, Skinner R. Health-related quality of life in survivors of BMT for paediatric malignancy: a systematic review of the literature. Bone Marrow Transplant. 2008;42(2):73-82.
|



